ロットによる濃度の差は「最初からの仕様」だった
コロナワクチンを巡っては、いろいろなことが起きていますが、今回は、米エポックタイムズの記事をご紹介したいと思います。
ファイザーは故意にワクチンに危険な成分を許可した (パート1) – mRNAの品質問題の調査
Pfizer Knowingly Allowed Dangerous Components in its Vaccines (Part 1)
Epoch Times 2023/02/19
ファイザーの COVID-19 ワクチンには、「短縮型 mRNA (truncated mRNA)」と呼ばれる一部を切り詰められた mRNA 断片が含まれている。これは生命を脅かす事象の問題に加えて、安全性として深刻な問題だ。
驚くべきことに、ファイザー社は、偽造された mRNA 分析レポートを複数の保健当局に提出していたことがわかった。
切断された mRNA の問題により、欧州医薬品庁(EMA)は、2020年12月のワクチンの条件付き承認の前に「重大な反対」を表明した。
何が起きていたのか?
これらの問題はどのように解決されたと考えられているのだろう。この 2部構成の連載記事では、この問題について詳しく説明し、人間の健康に対する潜在的な影響を調べる。
重要な事実の要約
・ファイザーの COVID-19 ワクチンには、切断された mRNA が含まれており、欧州医薬品庁はこれを「重大な異議」の理由としてフラグを立て、当初は承認の除外 (承認しないこと)を示した。
・ファイザーは、ワクチン中の切断された mRNA の有害な結果を調査していない。
・ファイザーは、実際の実験からではなく、デジタルで生成されたウエスタンブロット (※ タンパク質の特性を知るための基本的な実験手法)の数値をアメリカ食品医薬品局(FDA)と欧州医薬品庁に提出していた。
・この問題に関して、驚くべきことに、規制当局による措置は講じられていない。
・切断された mRNA は、誤って折り畳まれたスパイクタンパク質によって誘発される線維性血栓、自己免疫疾患、およびガンを含む、複数のワクチン関連の損傷に寄与する可能性がある。
・ファイザーのワクチンに関するこれらの問題は、ロットごとに劇的な製品品質の変動をもたらした可能性がある。これは、ワクチン接種者が経験する有害事象の違いを説明することができる。
・製薬会社や保健当局によるこのような無責任な行為の根本的な原因は、倫理の欠如だ。
スーパーマーケットに行って、子供のために 10本の牛乳を購入したい場合、通常は、これらの 10本のボトルの内容の物質と濃度は同じか類似していると想定するだろう。購入したボトルのうちの 5本がヨーグルトで満たされ、残りの 5本が水で薄められた牛乳で満たされているとは誰も予想しない。
ほとんどの店で購入する食品は、規制と品質管理により、私たちの期待を満たしている。
ワクチン製品を含む製薬業界にも同じ基準が存在する。
医薬品またはワクチン製品の異なるロット間で、主要成分の一貫した物理的および化学的パラメータが期待される。一貫性は、患者と消費者が医薬品の安全性と有効性に自信を持つことを可能にする基盤だ。
CMC プロセス (化学、製造、管理)には、製品の安全性とロット間の一貫性を確保するために従わなければならない製造慣行と製品仕様の定義が含まれる。これは、世界の保健当局が医薬品またはワクチンを承認するための必須の基準となっている。
従来の化学製品の品質管理は比較的簡単だが、mRNA などの生物学的製品の場合は、複雑になる。
切断されたmRNAとは何か? これが重要な理由
私たちの DNA には、ヌクレオチドで構成される遺伝子コードが含まれている。DNA はアミノ酸からなるタンパク質を作る。遺伝子コードとタンパク質の間には、 メッセンジャー RNA (mRNA) と呼ばれる「翻訳者」である架橋分子がある。
スパイクタンパク質をコードするファイザーワクチンの完全長 (※ スパイクタンパク質の RBD という部位と NTD という部位のすべてを作る) mRNA 配列は、長さが 4,284ヌクレオチドだ。
これは、スパイクタンパク質への翻訳を開始するための 5′ CAP 構造 (※ 細胞質mRNAなどの5’末端に見られる修飾構造)で構成されており、車の点火ボックスのように機能する。
翻訳可能領域の最後にあるオープンリーディングフレーム (※ タンパク質へと転写・翻訳される可能性のある DNA 配列)には、 車のブレーキのような終止コドン (※ タンパク質の生合成を停止させるために使われているコドン)がある。
切断された mRNA に「終止コドンが含まれていない場合」、「ブレーキ」シグナルを発することができない。つまり、タンパク質の翻訳プロセスが際限なく続くことになる。
このような切断された mRNA の停止コドンの欠落は、人間にとって非常に有害だ。有毒なタンパク質生成物の生成につながる可能性がある。
ファイザーの COVID-19 ワクチンには切断された mRNA が含まれている
欧州医薬品庁は、医薬品やワクチンを含むヨーロッパで人間が使用するすべての医薬品を承認する責任がある。人用医薬品委員会 (CHMP) は、同庁の意見の解釈を担当する欧州医薬品庁の委員会だ。
EMA/CHMP/448917/2021 という名称でコード化された欧州医薬品庁の評価報告書で、欧州医薬品庁はファイザーにワクチン製品の不純物に対処するよう要求した。
欧州医薬品庁の報告書は、この不純物を「短縮および修飾された mRNA」と表現している。
欧州医薬品庁へのファイザーのレポートは、 2021年 8月の欧州医薬品庁のレポートの14 ページのスクリーンショットに基づいて、下のグラフの「ピーク 1」で示されているように、ファイザーのワクチンに不純物が含まれていることを明確に示していた。
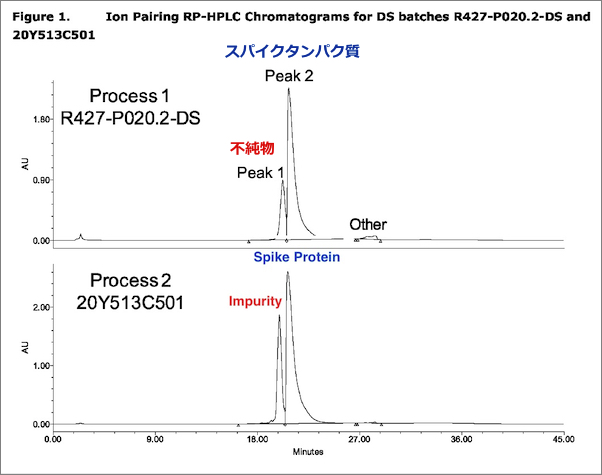
ファイザー社 mRNA ワクチンには不純物が含まれている。(欧州医薬品庁のデータ)
欧州医薬品庁は、ファイザーに対し、分子模倣メカニズムによる自己免疫状態を引き起こす可能性のある切断されたスパイクタンパク質/ペプチドまたは他のタンパク質/ペプチドを生成する可能性に関するデータを毎月提供するよう要求した。
期限は 2021年7月に設定されており、中間報告は 2021年3月までに提出する必要があった。
欧州医薬品庁は切断された mRNA を「重大な異議」としてフラグを立てた
2021年2月19日付けの EMA/707383/2020 という名称でコード化された評価報告書 15 ページの「製造業者、プロセス管理および特性評価」セクションには、以下のようにある。
「手続き中に、活性物質の製造のGMPステータスと、ロットリリースを目的とした最終製品の試験サイトに関連するいくつかの問題が強調された。 これらの問題は、メジャーオブジェクション (最大の異議)に分類された」
「メジャーオブジェクション 」は、欧州医薬品庁による正式な規制上の危険信号だ。主要な異議が未解決のままである場合、それらは販売承認の付与を妨げることになる。
切断された mRNA は、我々が上記で分析した2つの欧州医薬品庁のレポートによって提起された「主要な異議」として詳細に議論されてきた。
これらの生物学的薬剤が世界の人口に展開される前に、欧州医薬品庁の審査担当者は切断された mRNA の問題を特定し、それを「重大な異議」として取り上げた。
2022年6月、臨床試験に関するメディア「トライアル・サイト・ニュース」は、 ファイザー社と欧州医薬品庁の間の会議で提示された流出したスライドを明らかにする調査レポートを公開した。
欧州医薬品庁は、ファイザーがこれらの問題に対処することを要求した。
さらに、「意図したスパイクタンパク質 (S1S2) 以外の翻訳されたタンパク質が、切断された、および修飾された mRNA 種に起因する可能性に対処する必要があり、利用可能な場合は関連するタンパク質特性データを提供する必要がある」と通達した。
ファイザーは、ワクチンで切断された mRNA を認識していた
ファイザーの書類から、ファイザーは自社のワクチンに含まれる切断された mRNA を完全に認識していたことがわかる。
ほとんどの切断された mRNA は 1,500 ~ 3,500 ヌクレオチド長で、5′ CAP があり、ポリA配列 (※ 翻訳可能な成熟mRNAを生産するために不可欠な要素)と停止コドンがない。それらは、部分的なスパイクタンパク質に翻訳される。
このために、残念ながら、mRNA が翻訳の最後に到達しても、アミノ酸鎖は停止シグナルを与えられていないため、伸長を停止しない (※ タンパクの生産が止まらない)。
細胞内にはたくさんの mRNA があるが、停止信号がないため、理論的には、細胞内の別の mRNA が引き継ぎ、未完了の仕事を続け、「スパイクタンパク質」の生産を長引かせることになる。
同じスパイク mRNA が引き継がれると、複数の反復を持つ長期のスパイク様タンパク質が形成される。異なる mRNA が引き継がれると、未知の種類のタンパク質が作成される。
ファイザーはまた、切断された mRNA にポリA配列が欠けていることを認めた。
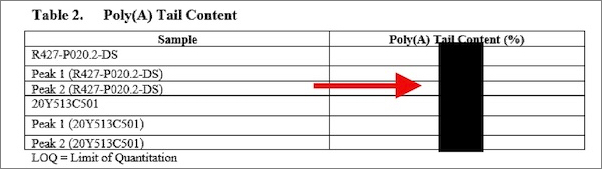
驚くべきことに、ダウンロードした欧州医薬品庁レポートでは、ピーク 1 の不純物の正確な割合が塗りつぶされていた。以下の注釈付きの表は、欧州医薬品庁の報告書の 17 ページのスクリーンショットに基づいている。
ファイザーはデジタル化されたウェスタンブロット図をアメリカ食品医薬品局と欧州医薬品庁に提出した
ウエスタンブロット法は、それを使用して特定のタンパク質を同定し、研究者が目的のタンパク質のサイズと存在量を確認できるようにするものだ。
誤ったスパイクタンパク質が予期せぬ傷害を引き起こす可能性があるという懸念から、欧州医薬品庁は、ファイザーに対し、切断された COVID-19 ワクチン RNA が断片タンパク質を生成しないことを実証する実験結果を提出するよう要求した。
欧州医薬品庁の要求は、ヒトでの使用を意図したあらゆる mRNA 製品について対処すべき基本的で最小限の懸念事項だ。
しかし、これは大量集団の予防ワクチンとして mRNA を使用した最初の例であるため、そのような品質の問題が発生したのもこれが初めてだ。
切断された mRNA のリスクを管理するための規制品質基準が以前にあったかどうかは不明だ。
これらの RNA の断片を特徴付ける唯一の方法は、配列決定によるもだ。ファイザーは、その報告書で切断された mRNA の詳細な配列を報告しておらず、おおよそのヌクレオチド数のみを報告している。
2020年12月、ファイザーは、アメリカ食品医薬品局 (FDA)に、 COVID-19 ワクチンによって誘発されたスパイクタンパク質のレベルを表すウエスタンブロットの画像を提供し、ワクチンは他のタンパク質を産生しなかったと主張した。
2020年の FDA レポートの 39ページのスクリーンショットに基づいて、ファイザーが生成した図の例を以下に示す。ファイザーは、mRNA ワクチンによって発現されたタンパク質のサイズを評価したことを表明し、次のように結論付けた。
ただし、グラフはデジタルまたはコンピューター化されたように見える。
(※) ここからは、その後に提出されたこの「ウエスタンブロット」というものの画像などの羅列になりますので、割愛します。
…ファイザーの偽のウエスタンブロットは、少なくとも アメリカ食品医薬品局、欧州医薬品庁、およびオーストラリア治療用品管理局 (TGA)を含む世界的な規制機関に提出された。
これらのウエスタンブロットが本物ではないことをどうやって知ることができるのか
ウェスタンブロッティング技術の最初のステップは、「ゲル電気泳動」と呼ばれる分子生物学的プロセスを使用してサンプル中のタンパク質を分離することだ。
異なるタンパク質は異なるサイズと分子量を持っているため、それらが同じ電場に置かれると、ランニングレースのように、一方の極から他方の極へと異なる速度で走る。
スタート地点では、400メートル走のレースのようにタンパク質が一列に並んでいる。
一定の時間が与えられると、小さなタンパク質は大きなタンパク質よりも速く移動し、徐々に異なるタンパク質が「バンド」と呼ばれる異なる場所で分離する。
これは、ランニングレースで起こることと似ている。 400メートルのランニングレースでは、さまざまなランナーが速度ごとに次々と分離される。
ウエスタンブロットの外観を決定する要因には、タンパク質の転写速度、インキュベーション (生まれる)時間、および抗体濃度が含まれる。
その結果、実際にウエスタンブロットが完璧になることはめったにない。常にいくつかの歪みがある。
(※) ここからもウエスタンブロットについての詳細が述べられているのですが、ちょっと専門的すぎて、わかりにくいですので、割愛させていただきます。
実験データがないため、決定的な結論を下すことはできない。それにもかかわらず、欧州医薬品庁はそれを承認した
欧州医薬品庁の同じレポートでは、次のようにも書いている。
ただし、切断された RNA と発現したタンパク質に関する実験データが不足しているため、決定的な結論を下すことができず、さらに特性を解明する必要がある。したがって、追加の特性データは、特定の義務 (SO1) として引き続き提供される。
偽のレポートを信頼できる実験データとして解釈し、規制当局の承認をサポートするものとして信頼する専門家がどこにいるだろうか。
それにもかかわらず、2021年8月の欧州医薬品庁レポートの 22 ページと 23 ページで、欧州医薬品庁はこれらの問題は解決済みと見なされていると述べた。
どのように解決されたと考えられるだろうか。この決定は、それらの偽のウエスタンブロットに基づいているのではないのか?
2020年12月12日、欧州医薬品庁は、ファイザーに条件付きの販売承認を付与した。
パート 2 では、この品質問題の意味と、ワクチン関連の損傷の潜在的な結果について説明する。
ここまでです。
なお、この記事を書いた方は、スイスのノバルティス本社の元上級医療科学専門家のユホン・ドン博士 (Yuhong Dong, MD, Ph.D)という方です。
専門的な部分ではわからない部分もあるのですが、ともかく承認の経緯がひどいものだったことは曖昧ではあってもわかります。
提供した側(ファイザー)も、承認する側(ここでは欧州医薬品庁)も、「この重大な問題をスルー」したのです。「解決した」としていますが、何も解決しないまま、承認に至ったのです。
ここでは欧州医薬品庁が取りあげられていますが、日本の厚生労働省も含めて世界中の規制当局が似たような感じだった可能性もあります。
そんなものが日本で 1億人、世界で数十億人に接種された。
なお、この記事で一番ショックを受けたのは以下の部分でした。
> 細胞内の別の mRNA が引き継ぎ……異なる mRNA が引き継がれると、未知の種類のタンパク質が作成される。
こんなんだと、「未知のタンパク質の生産が一生続いちゃうじゃないか」と……。